重组人胰岛素Chongzu Re nYidaosuRecombinant Human Insulin 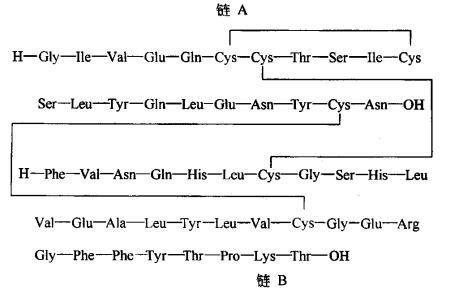
C
257H
383N
65O
77S
6 5807.69
本品为重组技术生产的由51个氨基酸残基组成的蛋白质。按干燥品计算,含重组人胰岛素(包括A
21脱氨人胰岛素)应为95.0%~105.0%。
每1单位重组人胰岛素相当于0.0347mg。
【制法要求】 本品为重组DNA技术产品,生产过程应符合《
人用重组DNA技未产品总论[1]》(三部总论)的要求.。
【性状】 本品为白色或类白色的结晶性粉末。
本品在水、乙醇和乙醚中几乎不溶,在稀盐酸和稀氢氧化钠溶液中易溶。
【鉴别】 (1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)取本品适量,加0.1%三氟醋酸溶液溶解并稀释制成每1ml中含10mg的溶液,取20μl,加0.2mol/L三羟甲基氨基甲烷-盐酸缓冲液(pH7.3)20μl、0.1%V8酶溶液20μl与水140μl,混匀,置37℃水浴中2小时后,加磷酸3μl,作为供试品溶液;另取重组人胰岛素对照品适量,同法制备,作为对照品溶液。照含量测定项下的色谱条件,以0.2mol/L硫酸盐缓冲液(pH2.3)-乙腈(90:10)为流动相A,以乙腈-水(50:50)为流动相B,按下表进行梯度洗脱。取对照品溶液和供试品溶液各25μl,分别注入液相色谱仪,记录色谱图,供试品溶液的肽图谱应与对照品溶液的肽图谱一致。
-----------------------------------
------------
时间(分钟) 流动相 A(%) 流动相 B(%)
-----------------------------------
------------
0 90 10
5 80 20
45 40 60
50 40 60
-----------------------------------
------------
【检查】 有关物质 取本品适量,加0.01mol/L盐酸溶液溶解并稀释制成每1ml中含3.5mg的溶液,作为供试品溶液。照含量测定项下的色谱条件,以0.2mol/L硫酸盐缓冲液(pH2.3)-乙腈(82:18)为流动相A,以乙腈-水(50:50)为流动相B,按下表进行梯度洗脱。调节流动相比例使重组人胰岛素主峰的保留时间约为25分钟,系统适用性试验应符合含量测定项下的规定。取供试品溶液20μl注入液相色谱仪,记录色谱图,按峰面积归一化法计算,含A
21脱氨人胰岛素不得大于1.5%,其他杂质峰面积之和不得大于2.0%。
-----------------------------------
--------------
时间(分钟) 流动相 A(%) 流动相 B(%)
-----------------------------------
--------------
0 78 22
36 78 22
61 33 67
67 33 67
-----------------------------------
--------------
高分子蛋白质 取本品适量,加0.01mol/L盐酸溶液溶解并稀释制成每1ml中约含4mg的溶液,作为供试品溶液。照分子排阻色谱法(通则0514)试验。以亲水改性硅胶为填充剂(5~10μm);以冰醋酸-乙腈-0.1%精氨酸溶液(15:20:65)为流动相;流速为每分钟0.5ml;检测波长为276nm。取重组人胰岛素单体-二聚体对照品,加0.01mol/L盐酸溶液溶解并稀释制成每1ml中约含4mg的溶液,取100μl注入液相色谱仪,重组人胰岛素单体峰与二聚体峰的分离度应符合要求。取供试品溶液100μl注入液相色谱仪,记录色谱图,扣除保留时间大于重组人胰岛素主峰的其他峰面积,按峰面积归一化法计算,保留时间小于重组人胰岛素主峰的所有峰面积之和不得大于1.0%。
干燥失重 取本品0.2g,在105℃干燥至恒重,减失重量不得过10.0%(通则0831)。
炽灼残渣 取本品约0.2g,依法检查(通则0841),遗留残渣不得过2.0%。
锌 精密称取本品适量,加0.01mol/L盐酸溶液溶解并定量稀释制成每1ml中约含0.1mg的溶液。另精密量取锌单元素标准溶液(每1ml中含Zn1000μg)适量,用0.01mol/L盐酸溶液分别定量稀释成每1ml中含锌0.2μg、0.4μg、0.6μg、0.8μg、1.0μg与1.2μg的梓标准溶液。照原子吸收分光光度法(通则0406第一法),在213.9nm的波长处测定吸光度,按干燥品计,含锌(Zn)量不得大于1.0%。
微生物限度 取本品0.3g,照非无菌产品微生物限度检查,微生物计数法(通则1105)检查,1g供试品中需氧菌总数不得过300cfu。
细菌内毒素 取本品,依法检查(通则1143),每1mg重组人胰岛素中含内毒素的量应小于10EU。
菌体蛋白残留量 取本品适量,依法检查(
通则3413[2]),每1mg重组人胰岛素中菌体蛋白残留量不得过10ng。
外源性DNA残留量取本品适量,依法检查(
通则3408[3]),每1剂量重组人胰岛素中宿主DNA不得过10ng。
生物活性 取本品适量,照胰岛素生物测定法(通则1211),每组的实验动物数可减半,实验采用随机设计,照生物检定统计法(通则1431)中量反应平行线测定随机设计法计算效价,每1mg的效价不得少于15单位。
【含量测定】 照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂(5~10μm);以0.2mol/L硫酸盐缓冲液(取无水硫酸钠28.4g,加水溶解后,加磷酸2.7ml、水800ml,用乙醇胺调节pH值至2.3,加水至1000ml)-乙腈(74:26)为流动相;流速为每分钟1ml;柱温为40℃;检测波长为214nm。取系统适用性溶液(取重组人胰岛素对照品,加0.01mol/L盐酸溶液溶解并稀释制成每1ml中含1mg的溶液,室温放置至少24小时)20μl,注入液相色谱仪,重组人胰岛素峰与A
21脱氨人胰岛素峰(与重组人胰岛素峰的相对保留时间约为1.3)的分离度不小于1.8,拖尾因子不大于1.8。
测定法 取本品适量,精密称定,加0.01mol/L盐酸溶液溶解并定量稀释制成每1ml中含0.35mg(约10单位)的溶液(临用新配)。精密量取20μl注入液相色谱仪,记录色谱图;另取重组人胰岛素对照品适量,同法测定。按外标法以重组人胰岛素峰与A
21脱氨人胰岛素峰面积之和计算,即得。
【类别】 降血糖药。
【贮藏】 遮光,密闭,在-15℃以下保存。
【制剂】 (1)重组人胰岛素注射液 (2)精蛋白重组人胰岛素注射液
关键字:重组 胰岛素
 C257H383N65O77S6 5807.69
C257H383N65O77S6 5807.69