| 通用名 | 盐酸莫索尼定片 |
| 曾用名 | |
| 英文名: | MOXONIDINE HYDROCHLORIDE TABLETS |
| 拼音名 | YANSUAN MOSUONIDING PIAN |
| 药品类别 | 抗高血压药 |
| 性状 | 本品为薄膜衣片,除去膜衣显白色。 |
| 药理毒理 | 莫索尼定是新型的中枢降压药,它是一种对咪唑啉I1受体具有高度亲和力的选择性激 动剂。根据不同的种属、组织和所用的配体,本品对咪唑啉I1受体的选择性比对α2肾上腺 素受体的选择性可高达600倍,在体内与中枢咪唑啉I1受体的结合明显与血压下降程度有关。 动物实验时用一种对咪唑啉受体位点有亲和力的α2肾上腺素受体拮抗剂预处理后,可抵消 本品引起的血压下降。 体外本品是一种α2肾上腺素受体选择性激动剂,比对α1肾上腺素受体结合强达288倍。 本品的降压作用与α2肾上腺素受体结合无明显关系。 小鼠药理实验显示:本品可减少自主活动次数,协同戊巴比妥促进小鼠睡眠,抑制中 枢神经系统活动;它在降压同时减慢心率,但对心电和呼吸频率及深度无明显影响。 大鼠的毒性实验显示:随所用剂量的增加,会出现松毛、少动和体重增长缓慢等一般 药物反应;尿液检查异常;肝酶的升高;病理组织学异常主要见于肾脏和心脏。停药四周以 后大部分异常指标可恢复。 小鼠的毒性实验显示:一次灌胃LD50(半数致死量)为190mg/kg;一次静脉注射LD50为 37mg/kg;对死亡小鼠组织学检查发现除左心室扩张和肺血管扩张充血外,其余脏器无明显 变化。 |
| 药代动力学 | 本品口服吸收较快,0.3~1小时血药浓度达峰值,生物利用度约为88%。本品没有首过 效应,58~60%的原型化合物经肾脏排泄,只有小于2%的药物经粪便排泄。小于15%的药 物在体内代谢,主要产物为4,5-脱氧莫索尼定和胍基衍生物,口服T1/2(消除半衰期)为2小 时左右。食物摄入不影响本品的药代动力学。 |
| 适应症 | 轻、中度原发性高血压 |
| 用法用量 | 本品应采用个体化用药原则。一般从最低剂量开始,即0.2mg,每天1次,于早晨 服用。若不能达到预期效果,可在三周内将剂量调至每日0.4mg,早晨服用或早晚各 0.2mg。单次剂量不得超过0.4mg或日剂量不超过0.6mg。 轻、中度肾功能不全者,单次剂量不得超过0.2mg或日剂量不超过0.4mg。 |
| 不良反应 | 治疗开始时可出现口干、疲乏和头痛等症状;偶见头晕、失眠和下肢无力感等。 极少产生胃肠道不适,个别有皮肤过敏反应。 |
| 禁忌症 | 1. 病窦综合症 2. II和III度窦房或房室传导阻滞 3. 心动过缓,休息状态下脉搏在每分钟50以下 4. 严重心律失常 5. 严重心功能不全 6. 不稳定型心绞痛 7. 严重肝病 8. 中度以上肾功能不全患者(肾小球滤过率在30ml/分钟以下) 9. 血管神经性水肿 10. 间歇性跛行、雷诺氏综合症、巴金森氏综合症、癫痫、青光眼等 |
| 注意事项 | 1. 轻度肾功能不全的患者,在服用本品时应监控其降压效果。 2. 对本品过敏时应停药。 3. 开车或操纵机器者应谨慎,可能影响其驾驶或操纵能力。 4. 与β阻断剂合用时,应先服用β阻断剂,然后隔一定时间再服本品。 5. 尽管在使用本品中迄今尚未发生过血压升降的异常变化,但建议长期服用本品时,勿 采取突然停药的措施。 |
| 孕妇及哺乳期妇女用药 | 孕妇及哺乳期妇女禁用。 |
| 儿童用药 | 16岁以下儿童禁用。 |
| 老年患者用药 | 老年患者须慎用,用初始剂量宜小,因为他们对药物的敏感性有时难以估计。 |
| 药物相互作用 | 1. 与β阻断剂合用时,开始时即产生降压,然后有较强的反跳现象出现。 2. 与其他降压药合用可增强本品的降压效果。 3. 与苄唑啉合用时,能削弱本品的降压作用。 4. 与酒精、镇静药或麻醉药合用时,能增强其降压效果。 |
| 药物过量 | 发生严重低血压可抬高下肢,补充血容量,如果无效,可缓慢静脉注射缩血管药物, 不断监测血压变化。 |
| 贮藏 | 遮光、密闭保存。 |
| 包装 | |
| 有效期 |
| 主要成分 | |||||||||
| 通用名 | 盐酸莫索尼定 | ||||||||
| 化学名 | 4-氯-5-(2-咪唑啉-2-氨基)-6-甲氧基-2-甲基嘧啶盐酸盐 | ||||||||
| 拼音名 | ANSUAN MOSUONIDING | ||||||||
| 英文名: | MOXONIDINE HYDROCHLORIDE | ||||||||
| CAS No. | |||||||||
| 结构式 | 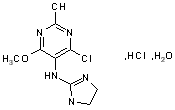 | ||||||||
| 分子式 | C9H12N5OCl·HCl·H2O | ||||||||
| 分子量 | 296.16 | ||||||||
| 规 格 | 0.2g | ||||||||