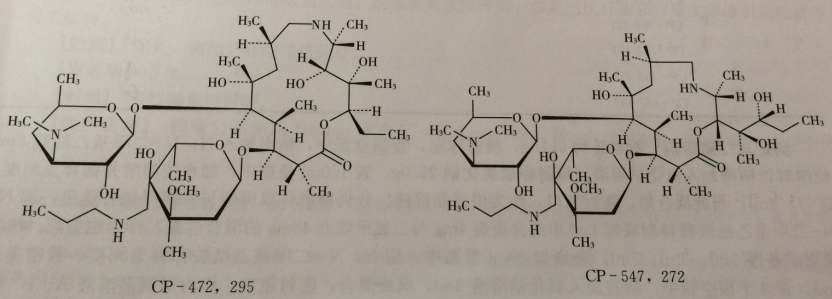
C41H79N3O12 806.23
本品为(2R,3S,4R,5R,8R,10R,11R,12S,13S,14R) -13- [ [2, 6-二脱氧-3-C-甲基-3-O-甲基-4-C-[(丙氨基)甲基]-a-L-核-已吡喃糖基]-氧]2-乙基-3,4,10-三轻基-5, 8, 10, 12,14-六甲基-11-[ [3, 4, 6-三脱氧-3-(二甲氨基)-β-D-木-已吡喃糖基] 氧]-1-氧杂-6-氮杂环十五烷-15酮(CP-472, 295)和(2R, 3R,6R,8R,9R,10S,11S,12R) -11- [ [2,6-二脱氧-3-C-甲基-3-O-甲基-4-C-[(丙氨基)甲基]-α-L-核-已吡喃糖基]-氧]-2- [(1R,2R)-1,2-二羟基-1-甲基丁基]-8-羟基-3, 6, 8, 10, 12-五甲基-9- [[3, 4, 6-三脱氧-3-(二甲氨基)-β-D-木-已吡喃糖基]-氧]-1-氧杂-4-氮杂环十三烷-13-酮(CP- 547, 272)。 按无水、无庚烷、无二氯甲烷物计算,含泰拉霉素两个异构体 (CP472, 295、 CP547, 272)之和应为 95.0%-103.0%。
【性状】本品为白色或类白色粉末。
本品在甲醇、丙酮、乙酸乙酯中易溶;乙醇中溶解。
比旋度 取本品适量,精密称定,加乙腈溶解并稀释制成每1ml中含40mg的溶液,在25°C时,依法测定(附录47页),按无水、无庚烷、无二氯甲烷物计算,比旋度为-22°--26°。【鉴别】(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)本品的红外光吸收图谱(附录25页)应与对照品的图谱一致。【检查】有关物质照含量测定项下方法测定。按峰面积归一化法计算,含CP-419, 471、CP- 471, 020 均不得过 2.0%,含CP-614, 159 不得过 1.5%, 含CP-702, 421不得过1.0%,其他单一杂质不得过0.5%,其他总杂质不得过3.0%,总杂质不得过6.0%。
CP-472, 295及有关杂质的相对保留时间| 化合物 | 相对保留时间 |
| CP - 615 595 | 0.21 |
| CP - 60 300 | 0.24 |
| CP - 60 273 | 0.44 |
| CP - 406 786 | 0.53 |
| CP - 467 096 | 0.59 |
| CP - 465 276 | 0.63 |
| CP - 547 272 | 0.68 |
| CP - 471 020 | 0.85 |
| CP - 472 295 | 1.00 |
| CP - 702 421 | 1.20 |
| CP - 614 159 | 1.42 |
| CP - 419 471 | 1.54 |
| CP - 667 992 | 2.05 |
庚烷与二氯甲烷取本品约0.16g,精密称定,置顶空瓶中,精密加人N,N-二甲基乙酰胺2ml 使溶解,精密加人氯化钠溶液(精密称取氯化钠25. 0g,置100ml量瓶中,加水使溶解并稀释至刻度,摇匀)3ml,涡旋混合后,密封瓶口,作为供试品溶液。分别精密称取庚烷与二氯甲烷各适量,加N,N-二甲基乙酰胺稀释制成每1ml中约含庚烷4mg与二氯甲烷0.48mg的混合溶液,作为C备液。精密量取贮备液1ml、3ml、5ml,分别置50ml量瓶中,用N,N-二甲基乙酰胺稀释至刻度,精密量取2ml,置3个顶空瓶中,精密加人氯化钠溶液3ml,涡旋混合,密封瓶口,作为对照品溶液A、B、C。照残留溶剂测定法(附录71页,第二法),以DB-624为固定液(或固定液相近)的毛细管柱为色谱柱;初始柱温为40°C,保持5分钟后,以每分钟升温2°C的速率升温至90°C,立刻以每分钟升温30°C 的速率升温至225°C,并保持2分钟;检测器为氢火焰离子化检测器(FID),检测器温度为260°C;进 样口温度为180°C;载气为氮气,顶空进样,顶空瓶平衡温度为105°C,平衡时间为60分沖。取对照品 溶液C顶空进样,各主峰之间的分离度均应符合要求。分别取供试品溶液和对照品溶液A、B、C顶空进样,记录色谱图,按标准曲线法以峰面积计算,应符合规定(庚烷不得过0.5%、二氯甲烷不得过0.06%).
注:供试品溶解后,加人氯化钠溶液后可能沉淀,但不会对分析结果产生显著影响。
水分 取本品,照水分测定法(附录69页,第一法A)测定,含水分不得过0.5%。细菌内毒素取本品0.5g,置试管中,加甲醇5ml,震荡溶解。依法检测(附录112页),每1mg 泰拉霉素中含内毒素的量应小于2EU。炽灼残渣 不得过0.1% (附录71页)。重金属 取炽灼残渣项下遗留的残渣,依法检查(附录66页,第二法),含重金属不得超过百万分之二十。【含量测定】照高效液相色谱法(附录32)测定。
色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂(YMC Pack Pro C18, 150mm×4.6mm,3um);甲醇-乙腈-0.05mol/L KH2P04 (pH值7.00) (45:25:30)为流动相;流速为每分钟2ml;柱温35°C±5°C;检测波长为205nm;CP-472, 295的理论板数不低于1000。对照品溶液中CP-651,595、CP-60, 300之间的分离度应大于1.05。杂质对照品贮备溶液的制备按下表制备杂质对照品贮备溶液。| 化合物 | 重量 | S瓶体积(ml) | 标识 |
| CP-651 595 | 5mg | 50 | A |
| CP-60 300 | 5mg | 100 | B |
对照品溶液的制备 取CP-472, 295对照品约100mg,精密称定,置50ml量瓶,加人稀释液约35ml,使溶解,精密量取杂质贮备溶液A、B各2ml,用稀释液稀释至刻度,即得。
供试品溶液的制备 取本品约0.1g,精密称定,置50ml量瓶中,用稀释剂溶解并稀释至刻度,摇匀,即得。测定法精密量取供试品溶液、对照品溶液各25ul,注人液相色谱仪,记录色谱图。按外标法,以峰面积计算,即得。【作用与用途】抗生素类药。用于治疗和预防对泰拉霉素敏感的溶血巴氏杆菌、多杀巴氏杆菌、睡眠嗜血杆菌和支原体引起的牛呼吸道疾病;胸膜肺炎放线杆菌、多杀巴氏杆菌和肺炎支原体引起的猪呼吸道疾病。
【贮藏】遮光,密闭,在凉暗处保存。
【有效期】3年。
【制剂】泰拉霉素注射液。
【生产企业】辉瑞公司美国 Groto n 生产厂(Eastern Point Road, Groto n, Connecticut 06340, USA)。
注:0.05mol/L磷酸二氢钾缓冲液(pH 7.00) 取KH2P04 6.8g,加水溶解并稀释至1000ml,用10mol/L氢氧化钾溶液调pH值至7.00±0.01。0.05mol/L磷酸二氢钾缓冲液(pH 5.50) 取KH2P04 6.8g,加水溶解并稀释至1000ml,用10mol/L氢氧化钾溶液调pH值至5.50士0.05。稀释液 甲醇-0.05mol/L KH2P04 (pH 5.50) (10:90)附加说明:1.本产品由辉瑞公司美国(Groto n生产厂Pfizer PGM. Groto n, USA)申请进口注册。2.本产品于2008年1月2日由农业部第957号公告批准进口注册并发布质量标准,证书号:(2008)外兽药证字05号。